A témakörhöz tartozó feladatokat itt találod.
Diffúzió és ozmózis

- A diffúzió biológiai jelentősége
- A részecskék belső energiájára visszavezethető hőmozgásán alapszik
- Eredménye az, hogy a részecskék a rendelkezésre álló térben teljesen egyenletesen fognak elhelyezkedni
- Alapja a sejtek életműködése szempontjából több fontos fizikai-kémiai folyamatnak
- Mindig a nagyobb koncentrációjú helyről a kisebb koncentrációjú hely felé
- Arányossági tényező: diffúziós állandó, függ a hőmérséklettől
- Biológiai jelentősége:
- Biológiai rendszrek mikroszkopikus anyagtranszport folyamatai
- Az anyagok sejtmembránain keresztül történő áthaladása
- Alapvető anyagcsere-folyamatok
- A vér és a tüdő közötti gázcsere
- Ingerületi folyamatok
- Felszívódás (pl. Gyógyszerek)
- Kémiai reakciók
- Sejtek közötti és sejtekben megvalósuló molekulamozgások
- Pl. Ozmózis
- Pl. Intracelluláris diffúzió, szerepe: biokémiai folyamatok, sejten belüli transzport, jelátvitel

- Az ozmózis biológiai jelentősége
- A víznek (oldószer) féligáteresztő hártyán keresztül történő diffúziója
- A féligáteresztő hártyán keresztül az oldószer a töményebb oldatba áramlik
- A folyamat addig tart, amíg az ionok koncentrációja meg nem egyezik, ekkor a rendszer dinamikus egyensúlyi állapotba kerül
- Mértéke: nyomásérték / ozmotikus nyomás
- A töményebb oldatra gyakorolt nyomással lehet a víz beáramlását megakadályozni -> a nyomás nagysága a két, félig áteresztő hártyával elválasztott oldat koncentrációkülönbségének függvénye
- Minél nagyobb a koncentrációkülönbség a két oldat töménysége között, annál erőteljesebb lesz a vízbeáramlás a hígabb oldatból a töményebb oldatba
- Minél töményebb egy oldat, annál nagyobb az ozmózisnyomása
- Biológiai jelentősége:
- Növényi és állati sejtek jelentős része vizes oldat, amelyet féligáteresztő hártya vesz körül
- Pl.: érett gyümölcsök széthasadása sok eső esetén
- Pl.: növényi nedvek felszívódáse a magas növények csúcsáig -> ozmózisnyomás
- Pl.: gyökérszőrök vízfelvétele
- Pl: túl sós ételek szomjúságot okoznak -> a szervezet vízfelvétellel igyekszik a nagy ozmózisnyomás hatását csökkenteni
- Emberi szervezet sejtjeinek oldatai a 0,9%os nacl-oldattal azonos ozmózisnyomásúak -> infúziók
- Pl.: dialízis -> a dializátorban kering a vér, a szűrő másik oldalán egy vérnek megfelelő összetételű sóoldat van -> a két teret elválasztó membránon keresztül átjutnak a vérből a salakanyagok
| Diffúzió | Ozmózis |
| Bármilyen típusú anyag | Csak víz mozgása |
| Bármilyen közegben (folyékony, szilárd, gáz) | Csak folyékony közegben |
| Nem igényel féligáteresztő hártyát | Féligáteresztő hártya |
| A diffúziós anyag kitölti a rendelkezésre álló teret | Az oldószer mennyisége nem lesz egyenlő a membrán két oldalán |
| Más részecskék jelenlététől függ | Az oldószerben oldott részecskék számától függ |
| A koncentráció kiegyenlítése az egész rendszerben | Az oldószer koncentrációjának kiegyenlítése |
Ha megértetted, itt , itt és itt tudod az ozmózis és a diffúzió közti különbséget gyakorolni, itt pedig példákat tudsz csoportosítani. Itt pedig egy tankocka-mátrixot találsz az ozmózis gyakorlásához.
Ozmózisos kísérletek, plazmolízis
- KÍSÉRLET: Egyszerű ozmózisos kísérletek
- 1. Üvegkád finom pórusú hártyával ellátva (állati bél, celofán) -> a vízmolekulák és a kisebb ionok átjutnak
- Egyik felébe desztillált víz, másik felőbe tömény nacl-oldat
- Később az üvegkád mindkét felőben azonos lesz a só koncentrációja
- 2. Üvegkád finom pórusú hártyával ellátva (állati bél, celofán)
- Egyik felébe desztillált víz, másik felébe tömény fehérje / cukoroldat
- A fehérje / cukormolekulák nem férnek át -> a vízmolekulák egyirányú diffúziója
- A vízmolekulák oda diffundálnak, ahol térfogategységként kevesebb van belőlük
Plazmolízis vizsgálata:
- Vöröshagyma bőrszöveti nyúzata -> kb. 1cm2-es felületű darab
- 5 percig 10%-os KCl-oldatba helyezni -> mikroszkóp alatt vizsgálni (10×20 nagyítás), KCl-oldattal lefedni!
- A nyúzatot egy másik, desztillált vizet tartalmazó óraüvegre helyezni -> öt perc
- -> mikroszkóp alatt vizsgálni (10×20 nagyítás), desztillált vízzel lefedni!
- Tapasztalat és magyarázat:
- 1. Vizsgálat: a 10%-os KCl-oldat töményebb, mint a sejt plazmája, a sejthártya pedig féligáteresztő tulajdonságú
- Ozmózis: a sejtplazma vizet veszít és zsugorodik, a sejthártya elválik a sejlfaltól
- A jelenség a plazmolízis, amely ozmózison alapszik
- 2. Vizsgálat: a sejtplazmánál hígabb oldatban az ozmózis iránya fordított
- A sejtplazma ismét kitölti a rendelkezésére álló teret a sejtfalon belül
- A jelenség a geplazmolízis
- 1. Vizsgálat: a 10%-os KCl-oldat töményebb, mint a sejt plazmája, a sejthártya pedig féligáteresztő tulajdonságú
- Hemolízis: a vörösvérsejteket hipotóniás oldatba helyezve megfelelően híg oldat esetén a vörösvérsejtek megduzzadnak és szétpukkadnak
- 1. Üvegkád finom pórusú hártyával ellátva (állati bél, celofán) -> a vízmolekulák és a kisebb ionok átjutnak

- A szervezet ozmotikusan aktív anyagainak szerepe az életfolyamatokban
- Vérfehérjék a visszaszívásban
- A vér ozmózisnyomásának kialakításában minden oldott molekuláris anyag részt vesz
- Kiemelkedő jelentősége a vérfehérjéknek van
- Albumin: nagy koncentrációban van jelen a vérben; mennyisége állandó
- A vér ozmózisnyomásának kialakításában minden oldott molekuláris anyag részt vesz
Nyirokképzés
- Nyirokkeringés: a zárt vérkeringési rendszerrel rendelkező gerincesek nyílt keringési rendszere
- Keringő anyag: nyirok, a vérplazmából származik
- A kapillárisok vékony falán a vérnyimásának hatására a plazma egy része átszűrődik -> a sejtek között szabadon mozgó szövetnedv, nyirok formájában található
- -> a vér sűrűsége nő -> a hajszálerek a vér növekvő ozmotikus nyomása miatt a kiszűrt nedv egy részét visszaszívják
- Mindig marad a szövetek között egy többé-kevésbé állandó koncentrációjú, főleg ionokat, esetleg kisebb molekulákat tartalmazó, fehérjementes nyirokmennyiség
- Vérfehérjék a visszaszívásban
Kolloidok
- A felületen való megkötődés biológiai jelentősége
- Adszorpció: valamennyi, felülettel rendelkező anyag a felületővel érintkező gáznemű vagy folyékony anyagokat megköti
- Valódi oldat: 1nm-nél kisebb részecskék oldószerben való elkeveredése
- Pl.: nacl vizes oldata
- Az oldott molekuláknak nincs felületük
- Felületi anyagmegkötésről sem beszélhetünk
- Nincs fajlagos felület
- Kolloid oldat: 1-500nm-es részecskék elkeverésekor
- A részecskék fajlagos felülete rendkívül nagy
- Fajlagos felület: a részecske tömegéhez viszonyított felület aránya
- A biológiai szempontból fontos makromolekulák legnagyobb rész eléri a kolloid mérettartományt
- Vizes közegben lévő kolloidok stabilitása -> nagy felület miatt
- Azonos anyagból álló szétoszlatott részecskék mindig azonos ionokat kötnek meg
- -> azonos töltés -> taszítani fogják egymást -> stabilitás megnő
- Szol: folyékony halmazállapotú
- Szuszpenzió: folyékony közegben szilárd részecskék
- Emulzió: folyékony közegben folyadékcseppek
- Gél: a kolloid részecskék hidrátburkuk hidrogénkötéseivel egymáshoz kapcsolódnak, egységes hálózatot képeznek -> a részecskék nem képesek elmozdulásra
- A szol óvatos lehűtéssel / lassú ütemű vízelvonással gél állapotba vihető
- Ha a gélekből fokozatosan távolítjuk el a vizet -> rugalmasságukat elvesztik, összezsugorodnak, kiszáradnak
- Koaguláció: a kolloid állapot megszűnése
- A kolloid részecskék stabilizáló ion- vagy vízburka megszűnik -> a diszpergált részecskék összetömörülnek, majd kicsapódnak a kolloid oldatból
- Denaturáció: a fahérje természetes szerkezetének elvesztése
- Az oldott fehérjék koagulációja a denaturáció következménye
- Vérben kolloidális mérettartományba esik:
- A vérplazma néhány fehérjéje, pl.: fibrinogén, albumin, globulinok
- A részecskék fajlagos felülete rendkívül nagy
- Diszperz rendszer: 500nm-nél nagyobb részecskék eloszlatása
- Vízbe szórt és azzal elkevert homokszemcsék
- A felületük arányában kötnek meg egy réteget a körülöttük lévő vízből
- A szilárd részecskék fajlagos felülete a tömegükhöz viszonyítva méretük növekedésével egyre kisebb lesz
- Valódi oldat: 1nm-nél kisebb részecskék oldószerben való elkeveredése
- Enzimműködés:
- Katalizáció: az enzimmolekulák felületén megtalálható centrom(ok)ban megköti a molekulá(ka)t és kialakul a komplex
- Az aktív centrum az enzimfehérje nagy molekulájának csak kis része
- Aminosavak: az átalakítandó anyag megkötésében játszanak szerepet -> nem egymás mellett helyezkednek el a polipeptidláncban
- Egymás közelébe kerülnek: az enzimmolekula feltekeredése során -> kialakul az aktív centrum speciális mintázata
- -> nagyfokú fajlagosság, csakis a meghatározott anyag átalakulását segítik elő
- Katalizáció: az enzimmolekulák felületén megtalálható centrom(ok)ban megköti a molekulá(ka)t és kialakul a komplex
- Adszorpció: valamennyi, felülettel rendelkező anyag a felületővel érintkező gáznemű vagy folyékony anyagokat megköti

Egy feladat a diszperz rendszerek csoportosításához

Talajkolloidok:
- Humusz és az anyagrészecskék kolloidális méretűek
- Ezek vízmegkötő képessége jelentős -> a humuszban és agyagban gazdag vályogtalajok sokkal több vizet tudnak megkötni és tartalékolni, mint a homoktalajok
- Kapillaritás: hajszálcsövesség
- A kolloidális méretű részecskék közötti hézagokban a víz gyorsan vándorol, illetve tartósan megmarad
- Magvak fagy- és szárazságtűrése: a sejek kötött víztartalma miatt
- Duzzadás: a kiszáradt gél képes újra vizet felvenni -> csírázás
Orvosi szén nagy felületi megkötőképességének kimutatása
- KÍSÉRLET: Mutassa ki az orvosi szén nagy felületi megkötőképességét festékoldattal. Tudja magyarázni és értelmezni a kísérletet, értse annak következményeit, alkalmazási lehetőségeit
- Lombikba kb. 200cm3 vörösbor / 5-6 csepp fukszinoldattal megfestett víz
- Adjunk hozzá szenet, majd keverjük össze
- Szűrjük le az oldatot -> a szűrlet színtelen lett
- Magyarázat:
- A vörös színanyag a szén nagy fajlagos felülete miatt a szénhez kapcsolódnak
- Abszorpció
- Következmények, alkalmazási leheőségek
- Gázmaszk
- Elvezetőcső nélküli konyhai elszívók
- Vákiimtechnikák
- Vegyipar, gyógyszeripar: különböző anyagok megkötése
- Ivóvíz-tisztítás
- A szén nagy aktív felülete miatt: ezen a felületen magukhoz kötik a baktériumokat, vírusokat, ezzel megakadályozva azok felszívódását a szervezetbe
Katalizátorok
Ez az okoslecke segít az enzimek és az aktiválási energia megértésében
- Aktiválási energia
- Az a minimális energia, ami egy kémiai reakció lezajlásához szükséges
- A reakció során a reaktáns molekulák összeütköznek, és a kémiai kötések megfeszülnek, elszakadnak és újak képződnek a termékek létrejöttekor
- -> aktivált komplex jön létre
- Alkalmazása biológiai folyamatokra
- Az élő szervezetekben az enzimek az aktiválási energiát csökkentve teszik lehetővé a biokémiai folyamatokat -> a katalizátorok a kémiai átalakulás számára új, kisebb aktiválási energiájú reakcióutat biztosíthatnak
- Anyagcsere alapja a biokémiai átalakulások -> energiamegmaradás és energiaminimumra törekvés elve

- Katalizátor
- Olyan anyag, amely növeli a kémiai átalakulások sebességét anélkül, hogy a folyamat következtében maradandóan megváltozna
- -> kisebb aktiválási energiájú reakcióutat nyit meg
- Katalizátorok jelenlétéven a reakciók más úton, alacsonyabb aktiválási energiájú részfolyamatokon keresztül játszódnak le -> növelik a reakciósebességet
- Alkalmazása biológiai folyamatokra
- Enzimek: biokatalizátorok, csak egyféle folyamatot katalizálnak
- Olyan anyag, amely növeli a kémiai átalakulások sebességét anélkül, hogy a folyamat következtében maradandóan megváltozna
Kromatográfiás kísérlet
- Kromatográfia
- Színnel írás, M.S.Cvet orosz botanikus -> fotoszintatikus pigmentek szétválasztása
- Szétválasztási művelet, melyet nagyon hasonló összetételű és szerkezetű anyagokból álló elegyek szétválasztására lehet felhasználni
- A szétválasztás alapját képező folyamatok szerint:
- Adszorpciós kromatográfia
- Az elegy összetevőinek adszorpciós képességének különbségén alapszik
- Ha az elegy mozog, az adszorpciós felület áll és az összetevők adszorpciója eltérő mértékű a felületen -> a rendszer komponenseire bontható
- Pl.: szűrőpapíron szétválasztani a fotoszintézisben szerepet játszó vegyületeket egymástól
- Megoszlási kromatográfia
- Az anyagkeveréket két egymással nem, vagy csak részlegesen elegyedő folyadékban oldják fel
- Az összetevők a kialakuló fázisokhoz való oldódásuknak megfelelően oszlanak el
- Ioncserélő kromatográfia
- A rendszerből ionok lépnek ki a rögzített felületre, amelynek anyagából hasonló töltésű ionok lépnek a folyékony bázisba
- Adszorpciós kromatográfia
- Mozgó- és állófázis jellege szerint:
- Folyadék-kromatográfia:
- Szilárd állófázis, egy ezzel nem elegyedő mozgófázis
- Gázkromatográfia:
- Gáz / gőz a mozgófázis, a megoszlás a gáz és szilárd vagy folyékony állófázis között alakul ki
- Vékonyréteg-kromatográfia:
- Állofázis: egy finom szemcsméretű kovasav-gél, allumínium-oxid, cellulóz
- Folyadék-kromatográfia:
- Egy leírt kromatográfiás kísérlet eredményének értelmezése, alkalmazása
- 1. Összezúzott lomblevél anyagaiból alkoholos kivonatot készítünk -> fotoszintetikus pigmentvegyületek (klorofill-a és –b, karotin, xantofill)
- Az elegyből egy cseppet szűrőpapírra cseppentünk
- A csepp a szűrőpapíron elfolyik és nagy színes folt keletkezik
- Folt száradása után többször tiszta kivonószert cseppentünk -> kiterjedtebb folt
- A fotoszintetikus fegyületek nem egyforma sebességgel vándorolnak az oldószercseppek hatására
- Legtávolabbra az az összetevő jut, amelyik legkevésbé kötődik a szűrőpapírhoz
- Karotin és xantofill
- Közelebb: klorofill-b
- Központhoz legközelebb: klorofill-a (legjobban kötődik)
- 1. Összezúzott lomblevél anyagaiból alkoholos kivonatot készítünk -> fotoszintetikus pigmentvegyületek (klorofill-a és –b, karotin, xantofill)
Enzimek
- Enzimek előfordulása (minden sejtben működnek)
- Enzimműködés lényege
- Enzimek: fehérjemolekulák, fajlagosak ->
- Kiindulási anyagok -> kötődnek az aktív centrumhoz (csak megfelelő térszerkezetű molekulák)
- A megkötött anyagok reakcióba lépnek egymással àtermékké alakulás
- A termék leválik az enzimről, mert térszerkezetük már nem illeszkedik az aktív centruméhoz ->
- Az enzim újabb kiindulási anyagokat köthet meg
- Enzimműködés optimális feltételei
- Optimális hőmérséklet:
- A kémiai folyamatok a hőmérséklet emelésével gyorsulnak
- Enzimek: csak egy határig, mert fehérjék -> a magas hőmérséklet tönkre is teheti a szerkezetüket -> nem tudnak összekapcsolódni az átalakítandó anyaggal
- Optimális pH:
- Minden enzimnek van egy optimális vegyhatása, amikor a leggyorsabban tud működni
- Optimális koenzim-koncentráció:
- Túl kevés koenzim: reakció lassul, túl sok koenzim: reakció nem gyorsul
- Optimális szubsztrát-koncentráció:
- Enzimek számához képest mennyi az átalakításra váró anyag
- Megfelelő ásványi anyagok jelenlése:
- Enzimaktivátorok (pl.: Ca, Mg, Cu, Zn)
- Optimális hőmérséklet:
- Enzimműködés optimális feltételei összefüggésben a szervezet jellemző értékeivel
- A hőmérséklet, pH, ozmotikus koncentráció érzékenysége -> az aktív centrum bonyolult szerkezetével függ össze
- A tényezők kismértékű megváltozása -> aktív centrum szerkezetét meghatározó aminosav-oldalláncok elmozdulnak -> az aktív centrum elveszti komplementer szerkezetét a szubsztrátéval
- Homeosztázis: szabályozott állandóság, amely jellemző a test hőmérsékletére / pH-értékére, az ozmotikus viszonyokra
- Testhőmérséklet: már kis hőmérsékletváltozás (tartós nyári meleg, láz) működési zavarokat okozhat az enzimeknél
- pH: kémhatás módosulása (pl. Gyors légzés, gyakori hányás) működési zavarokat okozhat az enzimeknél
- ozmotikus viszonyok
- A hőmérséklet, pH, ozmotikus koncentráció érzékenysége -> az aktív centrum bonyolult szerkezetével függ össze
- enzimhibán alapuló emberi betegség megnyilvánulásai
- tejcukor-érzékenység
- Oka: a laktáz hiánya / elégtelen működése -> tejcukrot bontja el
- A vékonybél nyálkahártyasejtjeiben található
- Laktóz: glükóz + galaktóz, egy kémiai kötés -> a kötés áthasítását végzi a bélben a laktáz enzim
- A kettős cukormolekula a bél hámsejtjein nem tud átjutni -> egyszerű cukrok fel tudnak szívódni és eljutnak a vérbe
- Emésztetlen tejcukor: ozmotikus hatás -> vizet szív a bél lumenébe -> hasmenés
- megelőzési lehetőségek
- tejcukorérzékenység:
- tejcukormentes diéta, laktáz enzim pótlása, tejcukortűrő képesség meghatározása
- tejcukorérzékenység:
- tejcukor-érzékenység
- Enzimműködés lényege
- ATP-bontó enzimek összefüggése az energiaigényes folyamatokkal
- Miozin
- Izomsejtek szerkezete ATP bontása során megváltozik
- Ennek során behúzza az aktinszálakat a miozinszálak közé -> izomrostok összehúzódása
- Na-K pumpa
- A sejtekből nátriumionokat távolít el, káliumionokat transzportál a sejtekbe
- A nyugalmi potenciál kialakítása -> idegsejteknél az ingerlékenység alapfeltétele
- Miozin
- ATP-szintézis összefüggése az egyenlőtlen ioneloszlásal
- Mitokondrium
- A mitokondrium az ATP-előállítás fő színtere
- Az ATP a terminális oxidáció folyamatában keletkezik
- A terminális oxidáció során a mitokondrium belső membránjának két oldalán a hidrogénionok egyenlétlen koncentrációja alakul ki
- Az ATP-t előállító enzim a belső membránban található, amely a hidrogénionok koncentrációkülönbségének kiegyenlítődését teszi lehetővé -> felszabaduló energiát beépíti az ATP-be
- Mitokondrium
Kísérlet az enzimműködéshez
- KÍSÉRLET: megtervezni és magyarázni az enzimműködéshez szükséges optimális kémhatást és hőmérsékletet bemutató kísérletet, eredmény értékelése
- Optimális hőmérséklet
- 4db kémcsőbe 2-2cm3 amiláz-oldat
- Egyéket felforraljuk
- Mindegyikbe 1-1cm3 keményítő-oldat, óvatosan összerázni
- A három, előzőleg fel nem forralt oldatot 0, 10 és 37 Celsius fokos vízfürdőbe
- 10 perc elteltével: 1-1 csepp minta mindegyik kémcsőből -> fehér csempelapra cseppenteni -> 1-1 csepp Lugol-oldatot hozzáadni
- Eredmény:
- Optimális hőmérséklet
| Hőmérséklet | 0 | 10 | 37 | 100 |
| Lugol-próba eredménye | +++ | + | — | +++ |
- Amelyik kémcsőben negatív a Lugol-próba eredménye, abban elbomlott a keményítő az enzim hatására
- Amelyikben kimutattuk a keményítőt, abben nem működött az enzim
- 0 fokon: nagy az aktiválási gát, a reakció nem megy végbe
- 10 fokon: lassú reakció
- 37 fokon: optimális mértékű reakció
- 100 fokon: irreverzibilisen denaturalizálta az enzimet, így elvesztette aktivitását
- pH-függés:
- hasonló kísérlet, ebben az esetben különböző kémhatás mellett kell vizsgálni
- 2×12 kémcsőbe 3cm3 fehérjeoldat
- Kémhatások beállítása: pH=1, pH=2, … pH=12 (jeweils 2 kémcső)
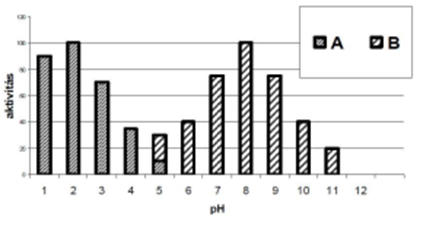
- Egyik kémcsősorozat: 1-1cm3 A emésztőnedv, másik kémcsősorozat: B emésztőnedv
- Emésztőnedv működési aktivitása a pH függvényében:
- Amelyikben kimutattuk a keményítőt, abben nem működött az enzim